Что такое рецидивная грыжа
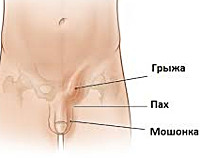
Рецидивная паховая грыжа — повторный выход органов брюшной полости через паховый канал после ранее выполненной герниопластики. Проявляется наличием выпячивания в области постгерниопластического рубца, тянущими болями в паху, дискомфортом при ходьбе, диспепсическими и дизурическими расстройствами. Диагностируется с помощью физикального осмотра, герниографии, сонографии пахового канала, МРТ области паха. Для лечения рекомендованы ненатяжные методы открытой и эндохирургической герниопластики. В редких случаях неблагоприятного течения заболевания у пожилых пациентов паховый канал ликвидируется.
Общие сведения
Рецидивное грыжеобразование — одно из наиболее частых осложнений паховых герниопластических операций. При использовании натяжных методов грыжесечения рецидив болезни возникает у 15-30% пациентов, переход на протезирующие техники позволил уменьшить этот показатель до 1-5%. Заболеванию более подвержены мужчины, что связано с большей распространенностью первичных грыж паха у представителей мужского пола и анатомическими особенностями строения их пахового канала. В полость грыжевого мешка рецидивного выпячивания обычно попадает петля тонкого кишечника, большой сальник, реже — мочевой пузырь, слепая, сигмовидная, нисходящая ободочная кишка, мочеточник, почка, у женщин — яичник, матка. Актуальность своевременной диагностики заболевания обусловлена риском ущемления.

Рецидивная паховая грыжа
Причины рецидивной паховой грыжи
Повторному образованию грыжевого выпячивания в паху способствуют технические нюансы предыдущей герниопластики, течение послеоперационного периода, индивидуальные особенности пациента. Специалисты в сфере герниологии, общей хирургии, гастроэнтерологии связывают формирование рецидивной грыжи с наличием таких этиологических факторов, как:
- Врачебные ошибки. Рецидивное грыжеобразование чаще всего вызвано неправильным выбором метода грыжесечения без достаточного учета анатомических особенностей строения пахового канала, срока существования дефекта, преморбидных особенностей пациента. Причиной повторной грыжи также могут стать нарушения техники операции, приводящие к неверному сопоставлению или натяжению сшиваемых тканей.
- Особенности послеоперационного периода. Вероятность расхождения швов, возникновения других видов несостоятельности стенок пахового канала после выполненного грыжесечения возрастает при развитии гнойно-воспалительного раневого процесса. Нормальному течению восстановительного периода препятствуют ранние нагрузки — поднятие тяжелых грузов, интенсивные занятия спортом с напряжением брюшного пресса.
- Реакция на установленный аллотрансплантат. Рецидивные грыжи при протезирующих методах пахового грыжесечения диагностируются редко, однако возрастающая популярность метода привела к увеличению общего количества таких осложнений. Повторное грыжевое выпячивание образуется при хроническом воспалении в зоне фиксации синтетического протеза к тканям или возникновении аутоиммунной реакции на материал имплантата.
- Сохранение предпосылок к грыжевой болезни. При наличии причин, спровоцировавших развитие первичной паховой грыжи, вероятен поздний рецидив. В группу риска входят больные пожилого возраста, астенического телосложения, страдающие заболеваниями, при которых повышается абдоминальное давление (запорами, аденомой предстательной железы, стриктурами уретры, бронхолегочной патологией с упорным кашлем).
По данным наблюдений, важную роль в формировании рецидивной грыжи играет наличие у пациента врожденной системной дисплазии соединительной ткани. Среди больных с повторным грыжеобразованием у 45-47% выявляются двухсторонние паховые грыжи, грыжевые выпячивания другой локализации (пупочные, бедренные, пищеводного отверстия диафрагмы). 19-20% пациентов страдает варикозной болезнью нижних конечностей, 3,5-4% — пролапсом митрального клапана, до 5% — дивертикулами мочевого пузыря, дивертикулезом тонкого кишечника. У 7-8% больных обнаруживаются стрии на коже.
Патогенез
Механизм формирования рецидивной паховой грыжи зависит от использованного ранее способа грыжесечения. При натяжных методах герниопластики разрушению восстановленных тканей обычно способствует прорезывание лигатурами. Патогенез грыжевого рецидива после пластики пахового канала с помощью синтетического имплантата основан на смещении протеза или его отрыве от точек фиксации. Выбор техники для укрепления передней стенки канала при слабости задней, недостаточное ушивание поперечной фасции, использование для пластики разволокненного апоневроза абдоминальных мышц, оставление широкого пахового промежутка, другие тактические и технические ошибки при выполнении различных видов герниопластики способствуют повторному грыжеобразованию с формированием нового грыжевого мешка в наиболее ослабленной зоне канала.
Классификация
Рецидивные грыжевые выпячивания паха принадлежат к категории приобретенных, отнесены к типу IV современной систематизации паховых грыж. На основании особенностей анатомического прохождения через структуры пахового канала выделяют прямые (IVa), косые (IVb), бедренные (IVc), комбинированные (IVd) повторные грыжи. Как и другие грыжевые образования, они могут быть вправимыми и невправимыми, неосложненными и осложненными. С учетом механизма грыжеобразования различают следующие виды рецидивных грыж по их локализации внутри пахового канала:
- Латеральный рецидив. Грыжевой дефект расположен рядом с глубоким паховым кольцом. Рецидивное грыжеобразование обусловлено нарушением техники обшивания семенного канатика.
- Срединный рецидив. Грыжа выходит в паховый канал в его средней части. Рецидивирование связано с разволокнением апоневроза или расхождением швов между ним и пупартовой связкой.
- Медиальный рецидив. Выпячивание выходит под кожу из наружного пахового отверстия. Возникает при укреплении передней стенки вместо ослабленной задней. Выявляется у 50-51% пациентов.
- Тотальный рецидив. Развивается в результате полного разрушения задней стенки канала. Отличается большими размерами и расположением по всей длине послеоперационного рубца.
- Ложный рецидив. Проявляется прямой рецидивной грыжей у больных, много лет назад прооперированных по поводу косой грыжи. Обнаруживается в 20-22% случаев повторного грыжеобразования.
Симптомы рецидивной паховой грыжи
Повторное возникновение заболевания чаще всего наблюдается в течение первых 3 лет после герниопластики. Основной признак рецидивной грыжи – появление в зоне послеоперационного рубца выпячивания, которое на начальных этапах может самопроизвольно вправляться в брюшную полость. Отмечаются постоянные тянущие боли в области паха, дискомфорт при ходьбе. По мере увеличения грыжи прогрессируют диспепсические расстройства (тошнота, снижение аппетита, хронические запоры, чувство неполного опорожнения кишечника). При попадании в грыжевой мешок части мочевого пузыря развиваются дизурические явления, боли при мочеиспускании. Общее состояние больных с рецидивом паховой грыжи обычно не нарушено.
Осложнения
При условии постоянной травматизации рецидивной грыжи может возникать пластический воспалительный процесс с формированием спаек, сращение содержимого грыжевого мешка с его стенками. Длительное течение заболевания вызывает нарушение моторной функции кишечника, задержку каловых масс, что чревато развитием острой кишечной непроходимости с сильными болями в животе, отсутствием стула, метеоризмом, многократной рвотой. Наиболее серьезное осложнение — ущемление паховой грыжи, которое приводит к нарушению кровоснабжения в петле кишки, ее некрозу, при отсутствии своевременной помощи зачастую осложняется перитонитом.
Диагностика
Постановка диагноза не представляет затруднений при наличии типичного выпячивания в паховой области и анамнестических сведений о проведении герниопластики. Сложности могут возникать при развитии болевого синдрома неясного генеза, который не сопровождается формированием пальпируемого образования, что требует проведения дополнительных диагностических мероприятий. Для верификации диагноза рецидивной паховой грыжи наиболее информативными являются:
- Физикальный осмотр. При помощи пальпации врач может определить наличие опухолевидного образования в области послеоперационного рубца, увеличивающегося во время кашля или натуживания. Проводится пальцевое исследование пахового канала, выявляется положительный симптом «кашлевого толчка».
- Герниография. При введении в полость брюшины контрастного вещества с помощью специальной иглы с мандреном удается обнаружить грыжу любых размеров, в том числе при ее атипичной локализации. Для улучшения визуализации грыжевого мешка проводят пробу Вальсальвы – просят больного натужиться в момент выполнения рентгенограммы.
- УЗИ пахового канала. Во время ультразвукового исследования оценивают локализацию и размеры рецидивной грыжи, визуализируют органы, расположенные в грыжевом мешке. С помощью сонографии можно детально изучить особенности анатомических структур паховой области, чтобы выбрать наиболее рациональный метод герниопластики.
- МРТ паховой области. Магнитно-резонансная томография имеет высокую чувствительность и специфичность, в 94% случаев позволяет достоверно исключить другую мышечно-сухожильную, абдоминальную и андрологическую патологию. Метод используется при недостаточной информативности других инструментальных исследований.
Лабораторные анализы крови и мочи имеют низкую диагностическую ценность, изменения показателей наблюдаются только при развитии осложнений рецидивной грыжи. Для исключения патологии со стороны органов малого таза проводится ультразвуковое исследование. Выполнение ирригоскопии, рентгенографии, МСКТ брюшной полости позволяет оценить состояние пищеварительного тракта. Дифференциальная диагностика производится с бедренной грыжей, паховой лимфаденопатией, туберкулезными холодными абсцессами, у мужчин – с гидроцеле, варикоцеле, гематоцеле, липомой семенного канатика, у женщин — с кистой круглой связки матки. Кроме осмотра хирурга-герниолога пациенту рекомендованы консультации гастроэнтеролога и онколога.
Лечение рецидивной паховой грыжи
Устранение повторно образовавшегося грыжевого дефекта выполняется хирургическим путем. Особенностями оперативных вмешательств при рецидивной грыже являются большая травматичность, необходимость глубокого проникновения в паховую область для надежного укрепления или воссоздания конкретных структур канала, широкое использование аллопластических материалов. При выборе метода герниопластики учитывают причины рецидива, состояние стенок, глубокого и наружного паховых отверстий, возраст пациента. Рекомендованными видами вмешательств являются:
- Открытая внебрюшинная аллопластика. Показана мужчинам репродуктивного возраста с предыдущей пластикой передней стенки. Сетчатым аллотрансплантатом укрепляется задняя стенка канала. При этом семенной канатик испытывает минимальное повреждающее воздействие, что позволяет предотвратить атрофию яичка и сохранить фертильность. В качестве альтернативы применяется полная реконструктивная обтурационная паховая герниопластика.
- Частичная обтурационная герниопластика. Рекомендована пациентам с ранее проведенной пластикой задней стенки и небольшими грыжевыми воротами. Отличается низкой травматичностью, возможностью проведения под местной анестезией, коротким реабилитационным периодом. Предполагает выполнение обтурации (пломбировки) грыжевых ворот моделированной частью протеза и предотвращение за счет этого выхода абдоминальных органов в просвет канала.
- Операция Лихтенштейна. Метод выбора при неоднократно рецидивирующей паховой грыже, больших размерах дефекта брюшной стенки, комбинированных образованиях. Преимущества вмешательства — отсутствие натяжения тканей за счет установки сетчатого протеза подходящей площади, низкий риск повторного рецидива (до 1%). При значительном разрушении канала в качестве альтернативной операции рекомендована его ауто- или аллопластическая реконструкция.
- Ликвидация пахового канала. Назначается в исключительных случаях больным старческого возраста, которым многократно выполнялась герниопластика. Первым этапом операции является орхиэктомия и удаление семенного канатика на стороне рецидивной грыжи, после чего грыжевые ворота ушиваются по стандартам лечения послеоперационных грыж. Радикальный подход предотвращает проведение повторных герниопластических вмешательств.
Вне зависимости от ранее использованных способов пластики открытые методы при наличии показаний могут заменяться эндохирургическими техниками (TAPP, TEP). На этапе предоперационной подготовки пациенту рекомендуется носить специальный бандаж, исключить факторы, способные повысить внутрибрюшное давление, — отказаться от физических нагрузок, проводить профилактику запоров, кашля.
Прогноз и профилактика
Исход заболевания зависит от наличия у больного сопутствующей патологии и своевременности диагностических мероприятий. Прогноз относительно благоприятный при небольшой паховой грыже, протекающей без осложнений. Риск многократного рецидивирования составляет от 18% до 43% в зависимости от типа проведенной операции. Профилактика рецидивных грыж включает тщательный выбор метода грыжесечения с учетом анатомических особенностей и состояния тканей, предупреждение развития послеоперационных гнойно-септических осложнений, терапию болезней, сопровождающихся увеличением внутрибрюшного давления, ограничение физических нагрузок.
Источник
Фото носит иллюстративный характер. Из открытых источников.
Грыжа пищеводного отверстия диафрагмы является одним из наиболее распространенных анатомо-топографических дефектов ЖКТ, сопровождающихся гастроэзофагеальной рефлюксной болезнью.
В настоящее время проведен достаточно объемный анализ эффективности первичных антирефлюксных вмешательств, определены методики выбора фундопликаций.
 Николай Сивец,
Николай Сивец,
заведующий хирургическим отделением
6-й ГКБ Минска,
профессор кафедры военно-полевой хирургии БГМУ,
доктор мед. наук
Суть операции — в коррекции пищеводного отверстия диафрагмы и формировании манжеты из дна желудка вокруг абдоминального отдела пищевода и кардии. Вмешательства по поводу грыжи пищеводного отверстия диафрагмы (ГПОД), как правило, выполняются лапароскопическим доступом, что уменьшает травматичность, сокращает срок нетрудоспособности и ускоряет реабилитацию.
Хирургическое лечение ГПОД в отдаленном послеоперационном периоде сопровождается достаточно высоким процентом рецидивов (от 11 % до 30 %). Хорошие и отличные результаты находятся в пределах 84–86 %. По данным ряда авторов, частота рецидивов после лапароскопической коррекции гигантских ГПОД (с площадью поверхности пищеводного отверстия диафрагмы более 20 см2) составляет 25–40 %.
Характерная особенность операции: наложение швов производится на уже разволокненные и подвергшиеся дегенерации диафрагмальные ножки. В результате ткани диафрагмы прорезываются, создаются условия для миграции наложенной фундопликационной манжеты в заднее средостение с развитием рецидива патологии. Попытка наложить швы на неизмененные ткани, захватывая при этом большое число диафрагмальных ножек, может привести к стойкой послеоперационной дисфагии в связи с чрезмерным сужением пищеводного отверстия диафрагмы.
Общеизвестны специфические механизмы и виды рецидивов: соскальзывание фундопликационной манжеты, или синдром телескопа, смещение манжеты в грудную полость выше диафрагмы, прорезывание швов манжеты или швов ножек диафрагмы, формирование параэзофагеальной грыжи. Наиболее часто отмечается скольжение фундопликационной манжеты выше диафрагмы при несостоятельности крурорафического шва. На втором месте рецидив вследствие разрыва и разволокнения диафрагмальной ножки. В литературе описаны механическая (проявляющаяся дисфагией) и функциональная (проявляющаяся изжогой) формы рецидива.
Для улучшения результатов хирургического лечения выполняется пластика пищеводного отверстия диафрагмы с применением сетчатого имплантата. Многие авторы считают, что использование сетки целесообразно только при больших размерах пищеводного отверстия диафрагмы, атрофии диафрагмальных ножек и в пожилом возрасте. Отношение к полипропиленовым сеткам в настоящее время весьма сдержанное. Ограниченность их применения в пластике пищеводного отверстия диафрагмы объясняется частыми осложнениями (длительной дисфагией в послеоперационном периоде, рубцовыми стриктурами, аррозией пищевода имплантатом и миграцией имплантата). При этом показания к постановке сетки не отработаны.
При повторно выполняемых операциях по поводу рецидивных ГПОД примерно в 70 % случаев используется фундопликация по Ниссену (Nissen), в 17–20 % — по Тупе (Toupet). Показания к повторному вмешательству: рецидивная ГПОД, особенно если отмечается повторное развитие рефлюкса, рефлюкс-эзофагита или других проявлений гастроэзофагеальной рефлюксной болезни (изжога, дисфагия, рвота, боли в грудной клетке). Доказано, что при повторных операциях снижается их эффективность, причем чем больше количество ранее перенесенных вмешательств, тем ниже эффективность каждого последующего. Данный факт требует тщательного подхода к определению показаний для рефундопликации. Чтобы точно установить, выполнима ли повторная операция, необходимо провести комплексное клиническое и рентген-эндоскопическое обследование.
Пациентка В., 69 лет, жительница Полоцка, госпитализирована в хирургическое отделение 6-й ГКБ Минска 29 мая 2017 года с рецидивной грыжей пищеводного отверстия диафрагмы.
Из анамнеза: в 2009 году оперирована в одной из клиник Витебска. Выполнена эндоскопическая операция в объеме задней крурорафии с установкой полипропиленовой сетки позади пищевода, фундопликация по Nissen. Спустя год возник рецидив ГПОД, больная была прооперирована повторно в той же клинике. Выполнена левосторонняя торакотомия, пластика пищеводного отверстия диафрагмы путем его ушивания. Около четырех лет после второй операции чувствовала себя удовлетворительно. Ухудшение состояния отмечает в течение последних двух лет. Стали беспокоить боли за грудиной, горечь во рту, отрыжка.
В апреле 2017 года пациентку консультировали в хирургическом отделении 6-й ГКБ Минска. Для проведения дифференциальной диагностики было рекомендовано дообследование. По месту жительства проведено комплексное клиническое, эндоскопическое и рентгенологическое обследование, в результате которого установлен клинический диагноз: рецидивная грыжа пищеводного отверстия диафрагмы. 29 мая пациентка госпитализирована, на следующий день прооперирована. Выполнена реконструктивная операция на пищеводе и желудке: лапаротомия, грыжесечение, передняя крурорафия, рефундопликация по Nissen. Длительность операции 3 часа 40 минут.
ИЗ ПРОТОКОЛА ОПЕРАЦИИ: верхне-срединная лапаротомия с обходом пупка слева. Ревизией органов брюшной полости установлено, что в брюшной полости имеется умеренный спаечный процесс после предыдущей операции. Большой сальник припаян к передней брюшной стенке, к печени, к ложу желчного пузыря. В подпеченочном пространстве слева, в области пищеводного отверстия диафрагмы, массивный спаечный процесс.
При дальнейшей ревизии установлено, что имеется рецидив грыжи пищеводного отверстия диафрагмы. Спайки разделены, выделены грыжевые ворота (диаметр около 5 см). Позади пищевода пальпируется сетчатый имплантат, который фиксирован к ножкам диафрагмы. К имплантату плотно фиксирована область пищеводно-желудочного перехода справа снизу. Попытка извлечения сетчатого имплантата сопровождалась травматизацией тканей и умеренным диффузным кровотечением.
Удалены две металлические скобки. Сетчатый имплантат оставлен на прежнем месте. Рассечена париетальная брюшина в области грыжевых ворот по левой стенке пищеводного отверстия диафрагмы. Мобилизован желудок в кардиальном отделе по малой кривизне, пересечены две короткие желудочно-селезеночные ветви по большой кривизне. Выделен абдоминальный отдел пищевода. Произведена мобилизация грудного отдела пищевода до 3 см. Пищевод смещен книзу. Признаков наличия фундопликационной манжеты по Nissen, сформированной на первой операции, не выявлено. Самоликвидация манжеты произошла, по-видимому, вследствие рассасывания шовного материала или прорезывания швов.
Учитывая вышеизложенное, сформировано пищеводное отверстие диафрагмы до 2,5 см в диаметре путем наложения двух швов на ножки диафрагмы впереди пищевода. Выполнена фундопликация по Nissen с формированием манжеты четырьмя швами. Желудок вместе с пищеводом фиксирован к правой ножке диафрагмы одним швом. Слева манжета фиксирована к диафрагме одним швом. Контроль гемостаза. Дренажная трубка в подпеченочное пространство к зоне пластики, вторая — над селезенкой. Из брюшной полости удалены инструменты. Послойный шов раны с механическим кожным швом. Повязка.
В первые дни после операции наблюдалась выраженная дисфагия. Пациентка могла принимать только жидкую пищу небольшими порциями. На 9-е сутки после операции выполнена контрольная ФЭГДС.
ЭНДОСКОПИЧЕСКАЯ КАРТИНА: пищевод свободно проходим, слизистая розовая, на ней творожистые микотические наложения. Кардия смыкается. Манжета сформирована в области кардии, без усилия проходима для эндоскопов последовательно 5,2 мм и 8,0 мм в диаметре. Тощаковое содержимое с обильной примесью желчи. Слизистая желудка очагово гиперемирована, отечна, рельеф сохранен. Пилорус, луковица и полость 12-перстной кишки без особенностей.
ЗАКЛЮЧЕНИЕ: состояние после герниопластики с фундопликацией по Nissen. Эритематозная гастропатия 1-й степени. Микоз пищевода.
В течение последующих четырех дней была продолжена консервативная терапия. Спустя две недели после операции, 13 июня, пациентка в удовлетворительном состоянии выписана на амбулаторное лечение.
Выводы
1. В современных условиях использование малоинвазивного эндоскопического метода оперативного лечения ГПОД является перспективным направлением в хирургии пищевода.
2. Для предупреждения рецидива ГПОД необходимо соблюдать основной принцип хирургического лечения: не только устранить грыжу, сузить грыжевые ворота, но и обязательно восстановить нормальное взаимодействие между желудком и пищеводом.
3. При несостоятельности крурорафических швов, прорезывании швов или расслоении диафрагмальной ножки задачей повторной операции является восстановление полноценности пластики и величины пищеводного отверстия диафрагмы.
4. Применение синтетических сетчатых эндопротезов при хирургической коррекции ГПОД считается удобным сиюминутным решением вопроса, но в случае рецидивирования грыжи это может помешать качественно выполнить реконструктивную операцию. Сетчатые имплантаты могут рассматриваться как вариант лишь при хирургическом лечении гигантских грыж пищеводного отверстия диафрагмы.
Источник


