Серома при паховой грыжи
Послеоперационная серома – это скопление серозной жидкости в зоне шва, обусловленное травматизацией мягких тканей. Является осложнением хирургических вмешательств. Рассасывается самостоятельно либо принимает хроническое течение. Проявляется припухл остью в области шва, чувством распирания, неприятными ощущениями и эффектом переливания жидкости при перемене положения тела. При крупных серомах наблюдаются нарушение общего состояния, субфебрилитет. Патология может осложняться инфицированием, формированием некроза. Лечение – пункции или дренирование с активной аспирацией на фоне медикаментозной терапии. В отдельных случаях требуются повторные операции.
Общие сведения
Послеоперационная серома (серома шва) – распространенное осложнение раннего послеоперационного периода. Чаще всего встречается в общей хирургии, маммологии, онкологии и пластической хирургии. По различным данным, частота образования клинически значимых сером после операций, сопровождающихся значительной отслойкой мягких тканей, колеблется от 0,8% до 80% и более. Осложнение может развиваться у пациентов любого возраста и пола, чаще встречается у женщин средней и старшей возрастной группы.
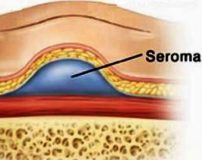
Послеоперационная серома
Причины
Серома является полиэтиологическим состоянием, рассматривается как осложнение обширных хирургических вмешательств. Некоторые специалисты придерживаются мнения, что скопление жидкости в проекции послеоперационной раны нельзя считать осложнением, поскольку оно представляет собой нормальный процесс заживления в фазе экссудации.
В подтверждение своей точки зрения ученые приводят данные ультразвуковых исследований, согласно которым послеоперационные серомы (в том числе – клинически незначимые) обнаруживаются у 100% пациентов. Основными провоцирующими факторами образования крупных сером, требующих проведения активных лечебных мероприятий, являются:
- значительная отслойка жировой клетчатки;
- большая раневая поверхность;
- грубые хирургические манипуляции с тканями (многочисленные разрезы, захват раздавливающим инструментом и пр.);
- чрезмерное использование коагуляции;
- большая толщина подкожной жировой клетчатки (более 5 см).
К числу предрасполагающих условий относят индивидуальные особенности организма, нарушения иммунитета, сахарный диабет и хронические соматические заболевания, негативно влияющие на процесс заживления раны. Чаще всего послеоперационные серомы образуются после абдоминопластики, герниопластики, маммопластики, мастэктомии, аппендэктомии, холецистэктомии. При использовании имплантатов имеет значение раздражение окружающих тканей и развитие асептического воспаления вследствие контакта с эндопротезом.
Патогенез
Существуют различные точки зрения на патогенез сером. Согласно наиболее популярной, обширные разрезы, отслойка мягкотканных структур, раздавливание или прижигание тканей и другие факторы вызывают значительные повреждения мелких лимфатических сосудов. Лимфатические сосуды тромбируются медленнее кровеносных, в результате лимфа долгое время изливается в ткани. На этапе экссудации жидкая часть крови выходит за пределы кровеносных сосудов, что увеличивает количество жидкости в тканях.
В полостях, возникших в области послеоперационной раны, скапливается соломенно-желтая жидкость, содержащая макрофаги, тучные клетки, лейкоциты и белковые фракции. В норме эта жидкость асептическая. При попадании микроорганизмов возможно нагноение с формированием абсцесса. Крупные скопления жидкости оказывают давление на окружающие ткани, нарушают кровоснабжение, вследствие чего могут образовываться участки некроза по краю швов.
Классификация
В клинической практике используют классификацию, в основе которой лежит необходимость и тактика лечения патологии. Согласно этой систематизации выделяют три группы послеоперационных сером:
- 1 группа. Асимптоматические образования, не требующие проведения лечебных мероприятий.
- 2 группа. Симптоматические серомы, для устранения которых достаточно пункций или активного дренирования.
- 3 группа. Симптоматические скопления жидкости, требующие проведения повторной операции.

Серома шва
Симптомы послеоперационной серомы
Маленькие образования не вызывают неприятных ощущений и нарушений общего состояния. Единственными признаками серомы являются припухлость и положительный симптом флюктуации в области послеоперационных швов. Иногда пациенты отмечают ощущение переливания жидкости во время изменения положения тела. Гиперемия кожи в зоне швов обычно отсутствует.
Больные с крупными серомами жалуются на неинтенсивную тянущую боль, чувство давления или распирания, которые усиливаются в положении стоя. В проекции швов выявляется валикообразная флюктуирующая припухлость. Длина припухлости обычно совпадает с длиной шва, ширина может варьироваться от 2-3 до 10 и более сантиметров. Возможны локальная гиперемия, слабость, утомляемость, повышение температуры тела до субфебрильных цифр.
Осложнения
Наиболее серьезным осложнением является нагноение серомы. При большом количестве жидкости формируются крупные абсцессы. Возможно расплавление подлежащих тканей с развитием перитонита. У некоторых больных развивается сепсис. Некрозы при серомах, как правило, протекают более благоприятно, захватывают небольшие участки тканей в области швов. Хронические серомы ухудшают качество жизни, существенно увеличивают период нетрудоспособности после операций.
Диагностика
Обычно серомы развиваются в период стационарного послеоперационного лечения, поэтому диагноз выставляется лечащим врачом. Диагностика базируется на данных объективного осмотра, при необходимости назначаются дополнительные исследования. Программа обследования может включать:
- Физикальный осмотр. В пользу серомы свидетельствует наличие ограниченного выбухания тканей в сочетании с положительным симптомом флюктуации. При отсутствии инфицирования гиперемия не выявляется или незначительная, пальпация малоболезненна. При инфицировании кожа багрово-синюшная, ощупывание резко болезненно, определяется плотный отек окружающих тканей.
- УЗИ мягких тканей. Показано для подтверждения диагноза при сомнительном симптоме флюктуации, для уточнения размеров крупных сером на этапе подготовки к хирургическому вмешательству. Свидетельствует о наличии полости, заполненной жидкостью.
- Лабораторные анализы. Для изучения характера содержимого серомы проводят цитологическое исследование. При подозрении на инфицирование выполняют бакпосев жидкости для определения возбудителя, назначают общий анализ крови для оценки выраженности воспаления.

Тактика лечения зависит от размеров серомы, наличия признаков инфицирования
Лечение послеоперационной серомы
Лечение осуществляется в стационарных условиях. При крупных образованиях, отсутствии признаков рассасывания показана комплексная терапия, включающая в себя консервативные и оперативные мероприятия.
Консервативная терапия
Целью консервативного лечения является снижение вероятности инфицирования, устранение асептического воспаления, уменьшение количества жидкости. Применяются медикаменты следующих групп.
- Антибиотики. При отсутствии нагноения пациентам для профилактики назначают препараты широкого спектра действия внутримышечно. При появлении признаков инфицирования план антибиотикотерапии корректируют с учетом чувствительности возбудителя.
- НВПС. Нестероидные противовоспалительные средства уменьшают проявления воспаления и количество жидкости, выделяющейся в просвет полости послеоперационной серомы. Возможно внутримышечное введение или пероральный прием.
- Глюкокортикоиды. Гормональные препараты устраняют асептическое воспаление, блокируют образование жидкости. Медикаменты вводят в полость серомы после удаления жидкости.
Хирургическое лечение
Тактика хирургического лечения определяется размерами серомы, эффективностью лечебных мероприятий на предыдущих стадиях. При неосложненных серомах возможны следующие варианты:
- Пункции. Наиболее простой способ удаления жидкости. Выполняется 1 раз в несколько дней, для полного излечения обычно требуется 3-7 пункций.
- Активная аспирация. При неэффективности пункций, значительном объеме серомы в полость образования устанавливают дренаж с устройством для активной аспирации.
- Реконструктивные операции. Показаны при упорном хроническом течении сером, отсутствии результата после лечения более щадящими способами.
При нагноившихся серомах производится вскрытие, дренирование гнойной полости. При образовании участков некроза проводят перевязки до отторжения струпа и полного заживления раны. Все хирургические методы применяют на фоне консервативной терапии.
Прогноз
Прогноз в большинстве случаев благоприятный. Небольшие серомы нередко рассасываются самостоятельно в течение 1-2 недель. Эффективность пункций при серомах на фоне плановых пластических и абдоминальных операций составляет около 90%. Реконструктивные вмешательства требуются редко. Процент нагноений незначительный, осложнение чаще развивается после экстренных операций, при наличии сопутствующей патологии, излишнем весе.
Профилактика
Профилактические мероприятия включают тщательную оценку риска хирургических вмешательств, детальное предоперационное обследование, соблюдение техники проведения операций. Хирургам необходимо воздерживаться от слишком широких разрезов, грубых манипуляций с тканями, чрезмерного использования коагулятора.
Источник
Изобретение относится к медицине, а именно к хирургии, и может быть использовано при лапароскопической паховой герниопластике у больных с прямой паховой грыжей.
Наиболее часто встречающимися осложнениями лапароскопической паховой герниопластики является псевдорецидив и серома. Эти осложнения связаны с тем, что перерастянутая поперечная фасция в области пахового промежутка пролабирует через наружное отверстие пахового канала после операции и вызывает опухолевидную деформацию, напоминающую рецидив грыжи. При скоплении тканевой жидкости между сетчатым эндопротезом и поперечной фасцией образуется серома, которая увеличивает сроки реабилитации, часто требует пункционного лечения, симулирует рецидив заболевания.
Наиболее распространенным способом профилактики описанных осложнений при лапароскопической паховой герниопластике является фиксация поперечной фасции в виде тяжа к связке Купера (Егиев В.Н., Воскресенский П.К. Грыжи. – М.: Медпрактика-М., 2015. – 480 с.). Способ осуществляется следующим образом. Делают Г-образный разрез брюшины паховой области, мобилизуют нижний лоскут брюшины, выделяют грыжевой мешок. Инструментом захватывают поперечную фасцию и фиксируют герниостеплером к связке Купера одной или двумя клипсами. Далее укладывают сетчатый эндопротез, закрывая все слабые места паховой области, фиксируют его и ушивают над ним брюшину. Способ прост в исполнении, но имеет недостатки. Для фиксации поперечной фасции используется дополнительные одну-две клипсы-спирали, что увеличивает количество металла в организме, а также способствует формированию хронического болевого синдрома у некоторых больных. Сетчатый эндопротез при описанном способе не прилегает к связке Купера на всем протяжении. Между ними имеет место интерпозиция поперечной фасции, что увеличивает вероятность рецидива.
Известен способ укрепления пахового канала при прямой паховой грыже путем пластики поперечной фасции эндопетлей (RU 2498778 C2, 20.11.2013.). Способ осуществляется следующим образом. Делают Г-образный разрез брюшины паховой области, мобилизуют нижний лоскут брюшины, выделяют грыжевой мешок. Инструментом захватывают поперечную фасцию и путем скручивания образуют тяж из неё, который лигируют эндопетлей у основания. Основным недостатком способа является то, что образуется достаточно большая масса тканей дистальнее эндопетли, которая подвергается некрозу в послеоперационном периоде, так как лишена кровоснабжения. Кроме того, в петлю при таком способе могут попасть элементы семенного канатика, которые расположены непосредственно на ней, а это может привести к некрозу яичка и развитию бесплодия у пациентов мужского пола.
Техническим результатом изобретения является профилактика серомы при эндовидеохирургическом лечении прямой паховой грыжи.
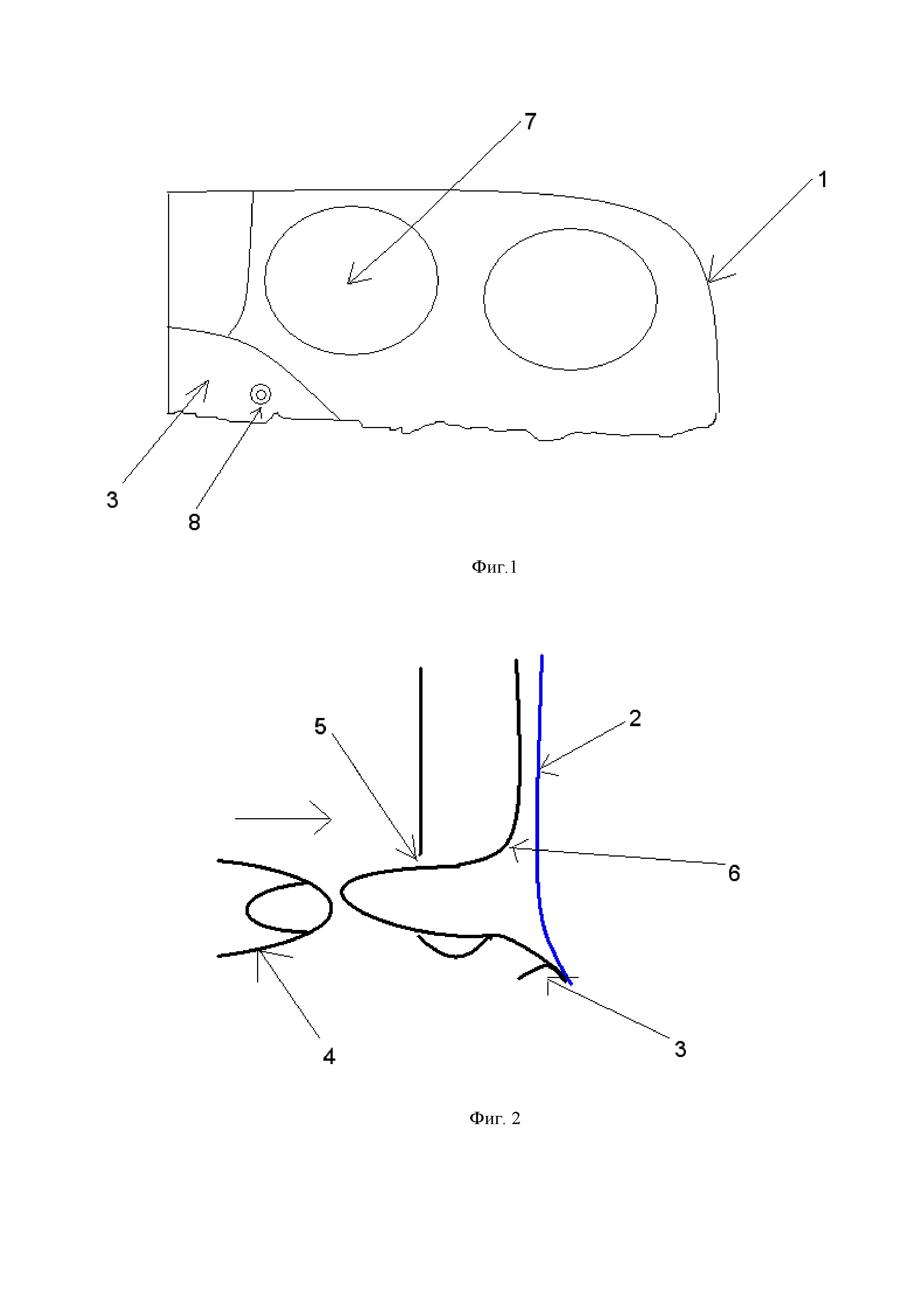
Способ заключается в следующем. Делают Г-образный разрез (1) брюшины паховой области, мобилизуют нижний лоскут брюшины, выделяют грыжевой мешок. В паховой области укладывают сетчатый эндопротез (2), который закрывает все слабые места в данной зоне, фиксируют к связке Купера (3) спиральной клипсой (8). Осуществляют мануальное вправление (4) поперечной фасции (6) в наружное отверстие пахового канала (5) таким образом, чтобы перерастянутая поперечная фасция (6) соприкасалась с сетчатым эндопротезом (2) в области медиальной паховой ямки (7). Далее накладывают один или два поверхностных шва (8), в зависимости от размера грыжевого мешка на поперечную фасцию в центре медиальной паховой ямки (7) непосредственно через эндопротез (2), не прекращая давление пальцем со стороны кожи, вяжут интракорпоральный узел.
Способ апробирован на 11 пациентах трудоспособного возраста 32-41 год. Длительные наблюдения в отдаленном послеоперационном периоде позволили выявить следующие неочевидные эффекты предложенного способа: ранний восстановительный период согласно классическим канонам герниопластики составляет не менее 14 дней, при использовании предложенного способа он составил не более 10 дней; избегание половой жизни в группе контроля не менее 20 дней, в группе исследования не более 11-12 дней.
При таком способе имеют место перечисленные ниже эффекты.
Ликвидируется остаточная полость между сетчатым эндопротезом и поперечной фасцией, что препятствует образованию серомы в этой области.
Увеличивается надежность фиксации сетчатого эндопротеза за счет его сшивания с поперечной фасцией.
Примеры.
Пример 1. Больной В., 76 лет. Поступил в плановом порядке с жалобами на опухолевидное образование в правой паховой области. На лапароскопической операции диагностирована прямая паховая грыжа. Выполнено выделение брюшины, грыжевого мешка. Поперечная фасция растянута. Полипропиленовый сетчатый эндопротез размерами 10х15 см расположен в паховой области и фиксирован к связке Купера. Поперечная фасция в центре медиальной паховой ямки фиксирована к протезу указанным способом. Дополнительной фиксации эндопротеза не потребовалось. Брюшина ушита интракорпоральным швом. Течение послеоперационного периода без особенностей. Контрольное ультразвуковое исследование на 3-и сутки после операции пред выпиской из стационара. Данных за наличие серомы нет. Больной осмотрен через 12 месяцев. Рецидива грыжи не отмечено, жалоб нет.
Пример 2. Больной К., 25 лет. Поступил в плановом порядке с жалобами на опухолевидные образования в паховых областях. На операции диагностирована двусторонняя прямая паховая грыжа. Выполнено выделение брюшины, грыжевых мешков с двух сторон. Поперечная фасция растянута. Полипропиленовые сетчатые эндопротезы размерами 10х15см каждый расположены в паховых областях и фиксированы к связкам Купера. Поперечная фасция в центре медиальной паховой ямки с двух сторон фиксирована к протезу указанным способом. Дополнительной фиксации эндопротезов не потребовалось. Брюшина ушита интракорпоральным швом. Течение послеоперационного периода без особенностей. Контрольное ультразвуковое исследование на 3-и сутки после операции пред выпиской из стационара. Данных за наличие сером с двух сторон нет. Больной осмотрен через 12 месяцев. Рецидива грыжи не отмечено, жалоб нет.
Описание к фигурам.
Фигура 1. Схема правой паховой области со стороны брюшной полости.
1 – Г-образный разрез брюшины
3 – связка Купера
7 – медиальная паховая ямка
8 – спиральная клипса
Фигура 2. Схема сагиттального среза паховой области .
2 – сетчатый эндопротез
3 – связка Купера
4 – палец
5 – наружное отверстие пахового канала
6 – поперечная фасция
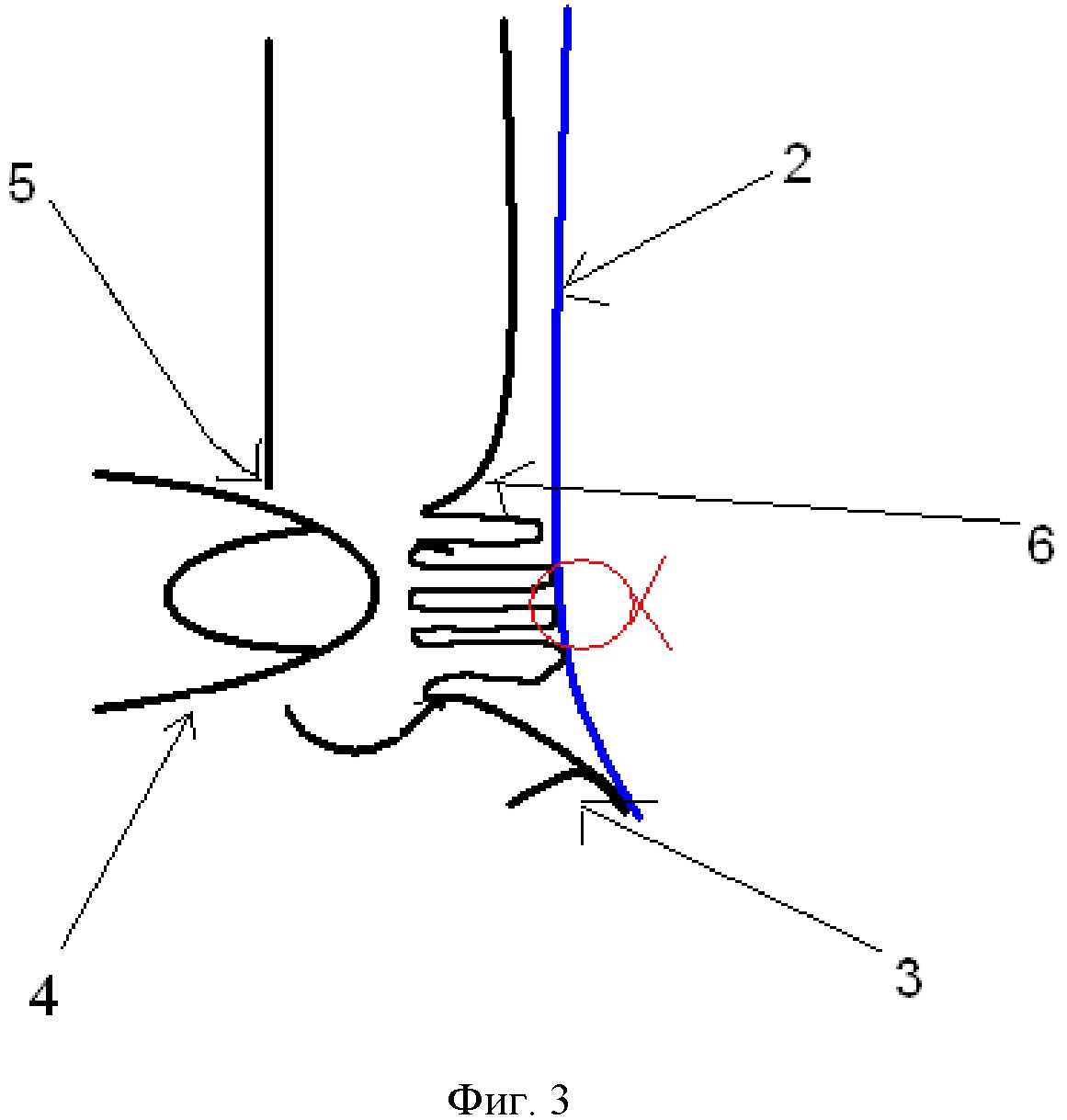
Фигура 3. Схема сагиттального среза паховой области после наложения шва.
2 – сетчатый эндопротез
3 – связка Купера
4 – палец
5 – наружное отверстие пахового канала
6 – поперечная фасция
8 — шов
Способ профилактики серомы при лапароскопической паховой герниопластике прямой паховой грыжи, при котором выполняют рассечение брюшины, мобилизуют нижний ее лоскут, выделяют грыжевой мешок, укладывают сетчатый эндопротез в паховой области, фиксируют его к связке Купера у медиального края спиральной клипсой, отличающийся тем, что осуществляют мануальное вправление поперечной фасции в наружное отверстие пахового канала до соприкосновения с сетчатым эндопротезом, фиксируют поперечную фасцию к эндопротезу в центре медиальной паховой ямки узловым интракорпоральным швом, ушивают разрез брюшины. 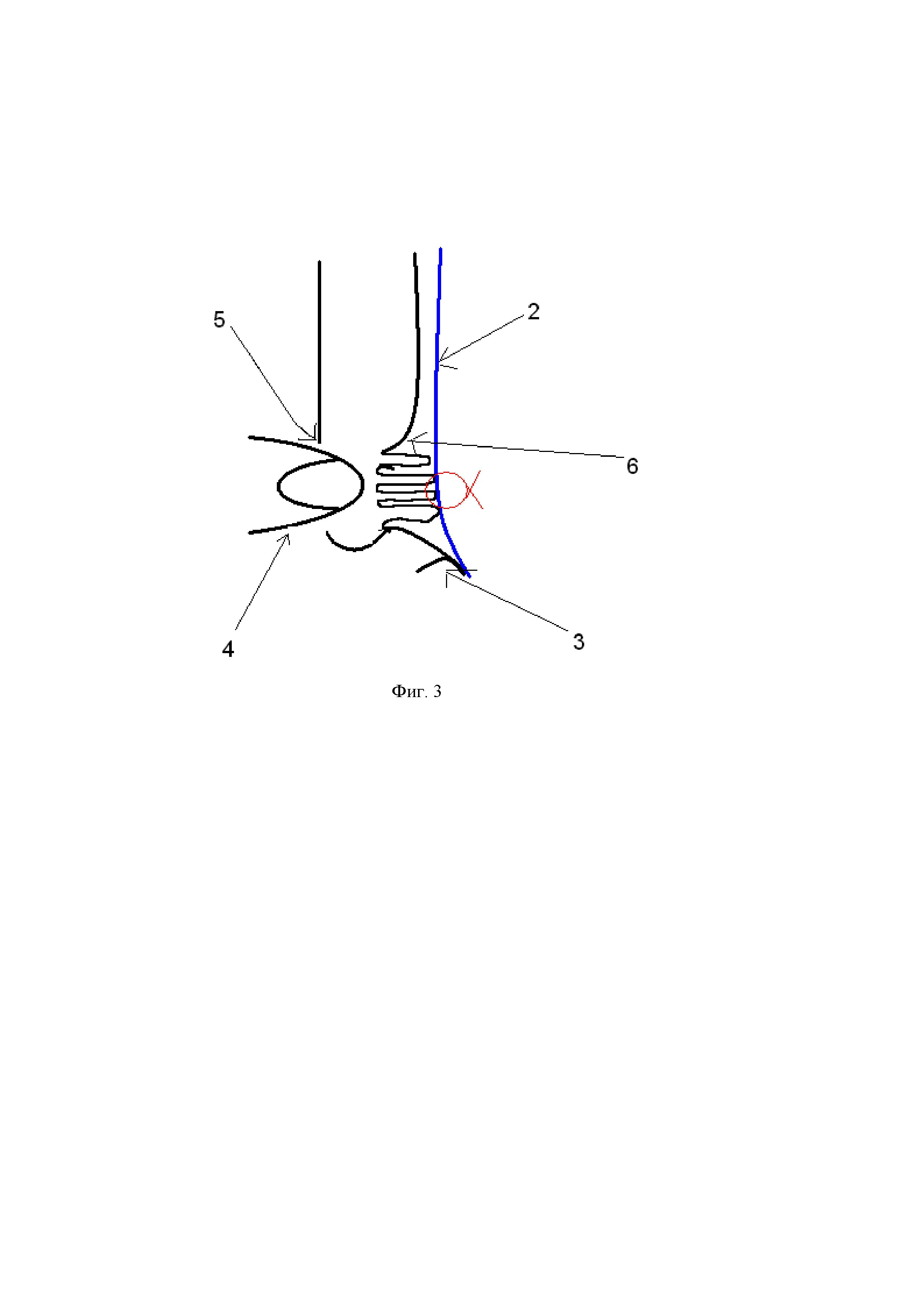

Источник
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения.
Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным
медицинским работником или студентом медицинского образовательного учреждения.
коронавирус
Уважаемые коллеги-врачи!
Профессиональный чат анестезиологов-реаниматологов Москвы открывает доступ к живой и непрерывно обновляемой библиотеке материалов, касающихся COVID-19. Библиотека ежедневно пополняется усилиями международного сообщества врачей, работающих сейчас в эпидемических зонах, и включает рабочие материалы по поддержке больных и организации работы лечебных учреждений.
Материалы отбираются врачами и переводятся волонтерами-переводчиками:
relaxandoit.ru
- Журналы
- Эндоскопическая хирургия
# 5, 2018
- Способ профилактики серомы во время т…
Авторы:
- Ю. М. Шептунов
Воронежский государственный медицинский университет им. Н.Н. Бурденко, Воронеж, Россия - П. В. Внуков
ГУЗ «Елецкая городская больница №2», Елец, Россия
Журнал:
Эндоскопическая хирургия. 2018;24(5): 3-6
Просмотрено:
1200
Скачано:
452
В последние годы стремительно возрастает популярность лапароскопической хирургии паховых грыж. Это связано с тем, что эффективность и без-опасность трансабдоминальной преперитонеальной пластики (ТАРР — transabdominal preperitoneal repair) были доказаны целым рядом исследований [1—3]. Существует множество официальных рекомендаций по лапароскопической паховой герниопластике [4]. В них четко регламентированы показания и противопоказания к данным операциям, особенности и границы диссекции преперитонеального пространства, характеристики требуемого имплантата и т. д. В то же время по ряду вопросов, таких как способ фиксации протеза и ушивания брюшины, возможность полной диссекции грыжевого мешка при пахово-мошоночных грыжах, необходимость использования электрокоагуляции, профилактика серомы и др., нет четкой регламентации, и выбор различных технических оперативных приемов остается за оперирующим хирургом [5—7].
Основные преимущества лапароскопического доступа — это ранняя реабилитация, гладкое течение раннего послеоперационного периода, возможность выполнения одновременной двусторонней пластики, в том числе при бессимптомной грыже [1, 3].
Одним из послеоперационных осложнений ТАРР, которое в целом мало влияет на конечный результат операции, риск рецидива, но в значительной степени нивелирует основные достоинства ТАРР, является серома. Поскольку в стандартном варианте операции выполняется широкая мобилизация брюшины с установкой сетчатого протеза площадью более 150 см2, вероятность образования скопления тканевой жидкости вокруг имплантата существует всегда. В то же время клинические проявления серомы чаще всего наблюдаются при операциях по поводу прямых паховых грыж [5, 6]. Это в свою очередь может нарушать процесс интеграции сетки в зоне пахового промежутка.
В связи с этим предложены различные варианты редукции фасциального мешка — анатомического субстрата клинически манифестной серомы. Наиболее широко распространенный вариант — фиксация измененной поперечной фасции пахового промежутка к связке Купера с помощью герниостеплера [8]. В связи с разной толщиной фасциальных структур этот способ не всегда обеспечивает надежную фиксацию. Кроме того, дополнительная скрепка увеличивает вероятность формирования синдрома хронической боли. Одновременно с этим интерпозиция ткани между имплантатом и гребенчатой связкой может также нарушать процесс интеграции протеза. Известен способ редукции фасциального мешка с помощью эндопетли [9]. Однако при этом образуется достаточно большой объем тканей, лишенных кровоснабжения, да и вероятность соскальзывания лигатуры велика.
Более сложный способ — ушивание фасциального мешка [10]. Это позволяет редуцировать поперечную фасцию и уменьшить паховый промежуток. Вместе с тем при наложении интракорпоральных швов достаточно сложно контролировать возникающее натяжение тканей, тем более в условиях пневмоперитонеума. А влияние этого натяжения на выраженность болевого синдрома при десуффляции, при активных движениях пациента в раннем послеоперационном периоде не изучено.
В связи с этим вопрос о необходимости и без-опасности пластики поперечной фасции в ходе ТАРР, а также оптимальном способе ее выполнения считается не решенным в настоящее время.
Цель исследования — разработка эффективного способа редукции фасциального мешка во время ТАРР при прямой паховой грыже.
Материал и методы
Исследование основано на анализе результатов выполнения 45 лапароскопических трансабдоминальных операций — ТАРР по поводу прямой паховой грыжи у 36 пациентов мужского пола. Основную группу составили 13 больных, которым выполнено 15 операций по разработанной методике (RU 2625445 C1), суть которой заключается в следующем. После выполнения стандартной мобилизации париетальной брюшины и помещения протеза размером 10×15 см в преперитонеальном пространстве фиксировали протез к связке Купера одной спиралью герниостеплером. Далее с помощью пальца ассистента осуществляли давление в проекции наружного отверстия пахового канала с тем, чтобы дно фасциального мешка соприкасалось с имплантатом. После этого накладывали от 1 до 3 интракорпоральных швов сквозь сетку с захватом поперечной фасции в области дна пахового промежутка. Ячеистая структура протеза позволяет визуализировать прошиваемые ткани достаточно четко. Дополнительной фиксации сетки, как правило, не требовалось. В случае большого размера грыжевого мешка предварительно уменьшали его полость одним интракорпоральным сборивающим швом в области дна. Показанием для данной манипуляции служили высота пахового промежутка 30 мм и более, а также отсутствие визуализации дна фасциального мешка при осмотре грыжевых ворот со стороны брюшины, что свидетельствовало о его большом размере. После этого сетчатый имплантат фиксировали в зоне медиальной паховой ямки интракорпоральным швом способом, описанным выше. Данный прием выполнен во время 6 операций. В качестве шовного материала применяли рассасывающиеся нити диаметром 4/0.
В группу контроля вошли 23 пациента, которым выполнено 30 операций по стандартной методике, описанной в национальных клинических рекомендациях. Из них во время 9 операций у пациентов с большой грыжей поперечная фасция фиксировалась к связке Купера одной или двумя спиралями с помощью герниостеплера.
Пациенты в контрольной и основной группах были сопоставимы по возрасту (медианы 58 и 59 лет соответственно) и срокам грыженосительства (от 2 до 48 мес). Девять грыж контрольной и 6 грыж основной групп оценены по размеру как большие, что составило 30 и 40% соответственно.
Оценка результатов проводилась в раннем послеоперационном периоде по стандартным критериям. Кроме того, через 3 сут всем больным было выполнено контрольное УЗИ паховой области, а также оценена интенсивность боли по визуальной аналоговой шкале. 28 пациентов осмотрены через 3—10 мес после операции с определением показателей качества жизни, связанного со здоровьем, по шкале MOS SF-36.
Статистическая обработка полученных результатов выполнена с использованием стандартного набора команд приложения MSExcel. Формат представления данных M±σ. Для выявления статистической значимости отличий применяли критерий Манна—Уитни.
Результаты
Среднее время операции в основной группе составило 61±9,8 мин, в контрольной группе — 52±10,7 мин, при статистически значимой разнице (р<0,05).
Сроки стационарного лечения в основной и контрольной группах различались незначительно: 6,0±0,9 и 6,3±1,1 койко-дня соответственно (р>0,05).
В раннем послеоперационном периоде тромбоэмболические и гнойно-воспалительные осложнения в обеих группах отсутствовали. Через 3 сут после операции в контрольной группе выявлено 5 сером, что составило 16,7%. Из них 3 образовались после операций без фиксации грыжевого мешка, а 2 были сопряжены с несостоятельностью фиксации вывернутой поперечной фасции к связке Купера, что определялось по характерной ультрасонографической картине. При этом в двух случаях протез в зоне пахового промежутка был окружен серомой с двух сторон. Четыре серомы имели выраженное клиническое проявление с выбуханием в паховой области, болевым синдромом и субфебрилитетом. В связи с этим выполнена пункция под УЗ-контролем 2—3-кратно с промежутком в 48 ч, после чего было отмечено значительное клиническое улучшение и дополнительные пункции не проводились. В основной группе ни клинически, ни при УЗИ серомы не выявлены (р<0,01).
Анализ выраженности болевого синдрома по 10-балльной визуальной аналоговой шкале показал, что в основной группе через 3 сут после оперативного вмешательства показатель составил 2,9±1,2 балла, в контрольной группе — 3,2±1,3 балла. Разница статистически достоверна (р<0,05).
Восемнадцать больных контрольной группы и 10 — основной группы осмотрены в отдаленном периоде. Рецидива ни клинически, ни при УЗИ передней брюшной стенки не обнаружено. Для оценки физического компонента здоровья выполнено анкетирование пациентов.
Показатель «физическое функционирование» в контрольной группе составил 93,3±6,4, в основной — 96±5,2 балла. Несмотря на более высокий показатель в основной группе, разница между группами по этому показателю статистически недостоверна (р>0,05). Показатель «ролевое функционирование» в контрольной и основной группах составил 80,1±20,2 и 85±21,1 балла соответственно. В этом случае также отвергнуть нулевую гипотезу об отсутствии отличий не удалось (р>0,05). Аналогично установлено, что разница между группами по показателю «общее состояние здоровья» статистически недостоверна. В контрольной группе он составил 85,9±2,1, в основной — 86,5±1,6 балла. В то же время значимые отличия между группами выявлены по показателю «интенсивность боли»: в основной группе его среднее значение — 95,2±7,7, в контрольной — 87,7±9,7 балла (р<0,05).
Обсуждение
Полученные предварительные результаты говорят о том, что ТАРР является эффективным и без-опасным методом хирургического лечения паховых грыж. В то же время это оперативное вмешательство при прямых грыжах может сопровождаться образованием серомы, морфологической основой которой является перерастянутая поперечная фасция пахового промежутка. Несмотря на отсутствие в контрольной группе рецидива заболевания, нагноения в зоне операции или увеличения продолжительности стационарного лечения, серома может удлинять общий срок полного восстановления и сказываться на удовлетворенности пациентов результатами операции. Предложенный способ редукции фасциального мешка одновременно выполняет и функцию фиксации протеза. Сохранение фиксации имплантата к поперечной фасции даже в случае развития серомы способствует интеграции протеза в слои передней брюшной стенки. Время, затрачиваемое на наложение шва, на несколько минут превышает время, требуемое для фиксирования поперечной фасции к связке Купера. Однако в основной группе этот промежуток времени уменьшается с увеличением количества операций, т. е. с выработкой мануального навыка. Способ, не сопровождаясь какими-либо специфическими периоперационными осложнениями, позволяет уменьшить количество сером, а также снизить выраженность болевого синдрома в раннем послеоперационном периоде. Сшивание поперечной фасции дна грыжевого мешка и сетчатого имплантата не приводило к формированию синдрома хронической боли у пациентов исследуемой группы.
В том случае, если выполняли ушивание поперечной фасции в условиях карбоксиперитонеума без фиксации ее к протезу, в раннем послеоперационном периоде возникали конфигуративные изменения имплантата (куполообразная деформация, особенно при высоком паховом промежутке, гофрирование протеза, минимальные перемещения), которые выявляли при ультрасонографическом обследовании. Эти изменения, по всей видимости, могут создавать дополнительные условия для возникновения серомы. Если же поперечная фасция просто была фиксирована к имплантату, никакие изменения его пространственной структуры не способствуют образованию преперитонеальных и префасциальных пространств. Этот прием позволяет редуцировать фасциальный мешок без малейшего натяжения практически у всех пациентов с прямой паховой грыжей.
Вывод
1. Перерастянутая поперечная фасция задней стенки пахового канала в случае прямой паховой грыжи со значительным объемом грыжевого мешка при ТАРР требует коррекции.
2. Одним из способов редукции фасциального мешка может быть подшивание его дна к сетчатому имплантату в области медиальной паховой ямки.
3. Описанный способ является безопасным и эффективным с точки зрения профилактики ранних послеоперационных осложнений, в частности серомы.
Авторы заявляют об отсутствии конфликта интересов.
Сведения об авторах
Шептунов Юрий Михайлович — д.м.н., профессор
Внуков Павел Владимирович — к.м.н., заведующий хирургическим отделением ГУЗ «Елецкая городская больница №2»; e-mail: pvnukov@yandex.ru; https://orcid.org/0000-0002-7396-7728
*e-mail: pvnukov@yandex.ru; https://orcid.org/0000-0002-7396-7728
Список литературы:
- Koju R, Koju RB, Malla B, Dongol Y, Thapa LB. Transabdominal Pre-peritoneal Mesh Repair versus Lichtenstein’s Hernioplasty. Journal of Nepal Health Research. 2017;15(2):135-140.
- https://doi.org/10.3126/jnhrc.v15i2.18202
- Scheuermann U, Niebisch S, Lyros O, Jansen-Winkeln B, Gockel I. Transabdominal Preperitoneal (TAPP) versus Lichtenstein operation for primary inguinal hernia repair — A systematic review and meta-analysis of randomized controlled trials. BMC Surgery. 2017;17(1):55. https://doi.org/10.1186/s12893-017-0253-7
- Wu JJ, Way JA, Eslick GD, Cox MR. Transabdominal Pre-Peritoneal Versus Open Repair for Primary Unilateral Inguinal Hernia: A Meta-analysis. World Journal of Surgery. 2018;42(5):1304-1311.
- https://doi.org/10.1007/s00268-017-4288-9
- Bittner R. Evidence-based TAPP technique. Chirurg. 2017;88(4):281-287. https://doi.org/10.1007/s00104-017-0387-2
- Köckerling F, Bittner R, Adolf D, Fortelny R, Niebuhr H, Mayer F, Schug-Pass C. Seroma following transabdominal preperitoneal patch plasty (TAPP): incidence, risk factors, and preventive measures. Surgical Endoscopy. 2018;32(5):2222-2231.
- https://doi.org/10.1007/s00464-017-5912-3
- Wong W, Lo OS, Law WL, eds. Topic: Inguinal Hernia — Fixation. Hernia. 2015;19(1):358-359.
- https://doi.org/10.1007/BF03355393
- Yang XF, Liu JL. Laparoscopic repair of inguinal hernia in adults. Annals of Translational Medicine. 2016;4(20):402.
- https://doi.org/10.21037/atm.2016.10.37
- Bittner R, Montgomery MA, eds. Update of guidelines on laparoscopic (TAPP) and endoscopic (TEP) treatment of inguinal hernia (International Endohernia Society). Surgical Endoscopy. 2015;29(2):289-321.
- https://doi.org/10.1007/s00464-014-3917-8
- Тарасенко С.В., Зайцев О.В., Копейкин А.А., Ахмедов Ш.И., Рахмаев Т.С. Способ укрепления задней стенки пахового канала при прямой паховой грыже путем пластики поперечной фасции эндопетлей. Вестник экспериментальной и клинической хирургии. 2015;8(3):310-313. https://doi.org/10.18499/2070-478X-2015-8-3-310-313
- Li J, Zhang W. Closure of a direct inguinal hernia defect in laparoscopic repair with barbed suture: a simple method to prevent seroma formation? Surgical Endoscopy. 2018;32(2)1082-1086.
- https://doi.org/10.1007/s00464-017-5760-1
Источник